
FABRAZYME 5 mg por oldatos infúzióhoz való koncentrátumhoz
ATC
Agalsidase beta
Hatóanyag
beta agalsidase
FABRAZYME 5 mg por oldatos infúzióhoz való koncentrátumhoz betegtájékoztatója
1. Milyen típusú gyógyszer a Fabrazyme és milyen betegségek esetén alkalmazható?
A Fabrazyme hatóanyaga a béta-agalzidáz - enzimpótló kezelésre alkalmazzák a Fabry-betegségben, amely esetén nincs α-galaktozidáz enzimaktivitás, vagy annak szintje kisebb a normálnál. Ha Önnek Fabry-betegsége van, akkor egy zsíros anyag, a globotriaozil-ceramid (GL-3) nem képes testének sejtjeiből eltávozni, így az elkezd a szerveiben, a vérerek falán lerakódni.
A Fabrazyme az orvosi diagnózis által igazoltan Fabry-betegségben szenvedő betegek hosszan tartó enzimpótló kezelésére javallt.
A Fabrazyme alkalmazása felnőttek, valamint 8 éves vagy annál idősebb gyermekek és serdülőkorúak számára javallt.
2. Tudnivalók a Fabrazyme alkalmazása előtt
Ne alkalmazza az Fabrazyme-ot:
- ha allergiás a béta-agalzidázra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Figyelmeztetések és óvintézkedések
Az Fabrazyme alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
Ha Önt Fabrazyme-mal kezelik, akkor az infúzióval összefüggő reakciók alakulhatnak ki Önnél. Az infúzióval összefüggő reakció minden olyan mellékhatás, amely az infúzió ideje alatt, vagy az infúzió beadása napjának végéig következik be (lásd 4. pont). Ha ilyen reakciót tapasztal, azonnal értesítse kezelőorvosát. Lehetséges, hogy további gyógyszereket kell kapnia az ilyen reakciók megelőzésére.
Gyermekek és serdülők
Nem végeztek klinikai vizsgálatokat a 0-4 éves gyermekekkel. A Fabrazyme biztonságosságát és hatásosságát 5-7 éves gyermekek esetében nem igazolták, így ennek a korcsoportnak semmilyen adag nem javasolható.
Egyéb gyógyszerek és a Fabrazyme
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni alkalmazni tervezett egyéb gyógyszereiről.
Tájékoztassa kezelőorvosát, ha bármilyen klorokin, amiodaron, benokin vagy gentamicin tartalmú gyógyszert szed. Ilyenkor fennáll a béta-agalzidáz-aktivitás csökkenésének elméleti kockázata.
Terhesség, szoptatás és termékenység
A Fabrazyme alkalmazása terhesség alatt nem ajánlott. A Fabrazyme terhes nőknél történő alkalmazásával kapcsolatban nincsenek tapasztalatok. A Fabrazyme alkalmazása szoptatás alatt nem ajánlott. A Fabrazyme átjuthat az anyatejbe. Nem végeztek vizsgálatokat arra vonatkozóan, hogy a Fabrazyme hatással van-e a termékenységre.
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Tilos gépjárművet vezetni vagy gépeket kezelni, amennyiben a Fabrazyme beadása közben vagy azt követően szédülést, álmosságot, forgó jellegű szédülést vagy eszméletvesztést tapasztal (lásd 4. pont). Először beszéljen kezelőorvosával.
A Fabrazyme nátriumot tartalmaz
A készítmény kevesebb mint 1 mmol (23 mg) nátriumot tartalmaz injekciós üvegenként, azaz gyakorlatilag "nátriummentes".
3. Hogyan kell alkalmazni a Fabrazyme-ot?
A Fabrazyme-ot vénás cseppinfúzió formájában (intravénás infúzió) alkalmazzák. A gyógyszer por formában kerül forgalomba, amelyet a beadás előtt steril vízzel fel kell oldani (lásd az egészségügyi szakembereknek szóló tájékoztatót a betegtájékoztató végén).
A gyógyszert mindig a kezelőorvosa által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát.
A Fabrazyme kizárólag olyan orvos felügyelete mellett alkalmazható, aki jártas a Fabry-betegség kezelésében. Kezelőorvosa azt javasolhatja, hogy Ön otthon kapja meg a kezelést, ha megfelel bizonyos feltételeknek. Ha szeretné, hogy az infúziót otthon kapja meg, kérdezze meg kezelőorvosát erről a lehetőségről.
A Fabrazyme javasolt adagja felnőtteknek testtömeg-kilogrammonként kéthetente egyszer 1 mg. Vesebetegségben szenvedő betegek esetén az adagolást nem szükséges módosítani.
Alkalmazása gyermekeknél és serdülőknél
A Fabrazyme javasolt adagja 8-16 éves gyermekeknek és serdülőknek testtömeg-kilogrammonként kéthetente egyszer 1 mg. Vesebetegségben szenvedő betegek esetén az adagolást nem szükséges módosítani.
Ha az előírtnál több Fabrazyme-ot alkalmazott
A testtömeg-kilogrammonkénti 3 mg-os adag még biztonságosnak tekinthető.
Ha elfelejtette alkalmazni az Fabrazyme-ot
Ha kimaradt Önnél egy Fabrazyme-infúzió, kérjük lépjen kapcsolatba kezelőorvosával.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A klinikai vizsgálatok során főként a gyógyszer betegeknek történő beadása alatt, vagy röviddel azután tapasztaltak mellékhatásokat (ezek az úgynevezett "infúzióval összefüggő reakciók"). Súlyos, életveszélyes allergiás reakciókról (anafilaxiás reakciókról) is beszámoltak néhány beteg esetében. Ha bármilyen súlyos mellékhatást tapasztal, azonnal forduljon kezelőorvosához.
Nagyon gyakori tünetek (10 betegből több mint 1-et érinthet) a következők: hidegrázás, láz, fázás, hányinger, hányás, fejfájás, szokatlan érzés a bőrön (pl. égető vagy bizsergő érzés). Kezelőorvosa dönthet úgy, hogy lassítja az infúzió sebességét, vagy további gyógyszereket ad az ilyen reakciók megelőzésére.
Egyéb mellékhatások listája:

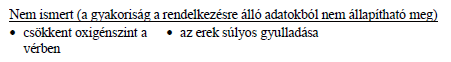
Néhány olyan betegnél, akik a javasolt adagot kapták a kezelés kezdetén, majd később csökkentett adagot kaptak hosszabb ideig, a Fabry-betegség néhány tünetéről gyakrabban számoltak be.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a https://mellekhatas.ogyei.gov.hu/ weboldalon. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Fabrazyme-ot tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A címkén feltüntetett lejárati idő (Felh.) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Felbontatlan injekciós üvegek
Hűtőszekrényben (2 °C - 8 °C) tárolandó.
Feloldott és hígított oldatok
Az elkészített oldat nem tárolható, hanem azonnal fel kell hígítani. A hígított oldatot 2 °C és 8 °C között legfeljebb 24 órán át lehet tárolni.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz az Fabrazyme?
- A készítmény hatóanyaga: 5 mg béta-agalzidáz injekciós üvegenként. A feloldást követően egy injekciós üveg 5 mg béta-agalzidázt tartalmaz milliliterenként
- Az egyéb összetevők:
-- mannit (E421)
-- nátrium-dihidrogén-foszfát-monohidrát (339)
-- dinátrium-hidrogén-foszfát-heptahidrát (339)
Milyen a Fabrazyme külleme és mit tartalmaz a csomagolás?
A Fabrazyme liofilizált, fehér vagy törtfehér por formájában kerül forgalomba. Feloldást követően tiszta, színtelen folyadék, idegen anyagtól mentes. Az elkészített oldatot tovább kell hígítani.
Kiszerelési egységek: 1 db, 5 db vagy 10 db injekciós üveg dobozonként. Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
A Fabrazyme hatóanyaga a béta-agalzidáz - enzimpótló kezelésre alkalmazzák a Fabry-betegségben, amely esetén nincs α-galaktozidáz enzimaktivitás, vagy annak szintje kisebb a normálnál. Ha Önnek Fabry-betegsége van, akkor egy zsíros anyag, a globotriaozil-ceramid (GL-3) nem képes testének sejtjeiből eltávozni, így az elkezd a szerveiben, a vérerek falán lerakódni.
A Fabrazyme az orvosi diagnózis által igazoltan Fabry-betegségben szenvedő betegek hosszan tartó enzimpótló kezelésére javallt.
A Fabrazyme alkalmazása felnőttek, valamint 8 éves vagy annál idősebb gyermekek és serdülőkorúak számára javallt.
2. Tudnivalók a Fabrazyme alkalmazása előtt
Ne alkalmazza az Fabrazyme-ot:
- ha allergiás a béta-agalzidázra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Figyelmeztetések és óvintézkedések
Az Fabrazyme alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
Ha Önt Fabrazyme-mal kezelik, akkor az infúzióval összefüggő reakciók alakulhatnak ki Önnél. Az infúzióval összefüggő reakció minden olyan mellékhatás, amely az infúzió ideje alatt, vagy az infúzió beadása napjának végéig következik be (lásd 4. pont). Ha ilyen reakciót tapasztal, azonnal értesítse kezelőorvosát. Lehetséges, hogy további gyógyszereket kell kapnia az ilyen reakciók megelőzésére.
Gyermekek és serdülők
Nem végeztek klinikai vizsgálatokat a 0-4 éves gyermekekkel. A Fabrazyme biztonságosságát és hatásosságát 5-7 éves gyermekek esetében nem igazolták, így ennek a korcsoportnak semmilyen adag nem javasolható.
Egyéb gyógyszerek és a Fabrazyme
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni alkalmazni tervezett egyéb gyógyszereiről.
Tájékoztassa kezelőorvosát, ha bármilyen klorokin, amiodaron, benokin vagy gentamicin tartalmú gyógyszert szed. Ilyenkor fennáll a béta-agalzidáz-aktivitás csökkenésének elméleti kockázata.
Terhesség, szoptatás és termékenység
A Fabrazyme alkalmazása terhesség alatt nem ajánlott. A Fabrazyme terhes nőknél történő alkalmazásával kapcsolatban nincsenek tapasztalatok. A Fabrazyme alkalmazása szoptatás alatt nem ajánlott. A Fabrazyme átjuthat az anyatejbe. Nem végeztek vizsgálatokat arra vonatkozóan, hogy a Fabrazyme hatással van-e a termékenységre.
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Tilos gépjárművet vezetni vagy gépeket kezelni, amennyiben a Fabrazyme beadása közben vagy azt követően szédülést, álmosságot, forgó jellegű szédülést vagy eszméletvesztést tapasztal (lásd 4. pont). Először beszéljen kezelőorvosával.
A Fabrazyme nátriumot tartalmaz
A készítmény kevesebb mint 1 mmol (23 mg) nátriumot tartalmaz injekciós üvegenként, azaz gyakorlatilag "nátriummentes".
3. Hogyan kell alkalmazni a Fabrazyme-ot?
A Fabrazyme-ot vénás cseppinfúzió formájában (intravénás infúzió) alkalmazzák. A gyógyszer por formában kerül forgalomba, amelyet a beadás előtt steril vízzel fel kell oldani (lásd az egészségügyi szakembereknek szóló tájékoztatót a betegtájékoztató végén).
A gyógyszert mindig a kezelőorvosa által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát.
A Fabrazyme kizárólag olyan orvos felügyelete mellett alkalmazható, aki jártas a Fabry-betegség kezelésében. Kezelőorvosa azt javasolhatja, hogy Ön otthon kapja meg a kezelést, ha megfelel bizonyos feltételeknek. Ha szeretné, hogy az infúziót otthon kapja meg, kérdezze meg kezelőorvosát erről a lehetőségről.
A Fabrazyme javasolt adagja felnőtteknek testtömeg-kilogrammonként kéthetente egyszer 1 mg. Vesebetegségben szenvedő betegek esetén az adagolást nem szükséges módosítani.
Alkalmazása gyermekeknél és serdülőknél
A Fabrazyme javasolt adagja 8-16 éves gyermekeknek és serdülőknek testtömeg-kilogrammonként kéthetente egyszer 1 mg. Vesebetegségben szenvedő betegek esetén az adagolást nem szükséges módosítani.
Ha az előírtnál több Fabrazyme-ot alkalmazott
A testtömeg-kilogrammonkénti 3 mg-os adag még biztonságosnak tekinthető.
Ha elfelejtette alkalmazni az Fabrazyme-ot
Ha kimaradt Önnél egy Fabrazyme-infúzió, kérjük lépjen kapcsolatba kezelőorvosával.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A klinikai vizsgálatok során főként a gyógyszer betegeknek történő beadása alatt, vagy röviddel azután tapasztaltak mellékhatásokat (ezek az úgynevezett "infúzióval összefüggő reakciók"). Súlyos, életveszélyes allergiás reakciókról (anafilaxiás reakciókról) is beszámoltak néhány beteg esetében. Ha bármilyen súlyos mellékhatást tapasztal, azonnal forduljon kezelőorvosához.
Nagyon gyakori tünetek (10 betegből több mint 1-et érinthet) a következők: hidegrázás, láz, fázás, hányinger, hányás, fejfájás, szokatlan érzés a bőrön (pl. égető vagy bizsergő érzés). Kezelőorvosa dönthet úgy, hogy lassítja az infúzió sebességét, vagy további gyógyszereket ad az ilyen reakciók megelőzésére.
Egyéb mellékhatások listája:

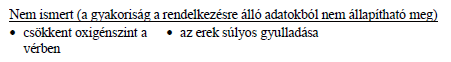
Néhány olyan betegnél, akik a javasolt adagot kapták a kezelés kezdetén, majd később csökkentett adagot kaptak hosszabb ideig, a Fabry-betegség néhány tünetéről gyakrabban számoltak be.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a https://mellekhatas.ogyei.gov.hu/ weboldalon. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Fabrazyme-ot tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A címkén feltüntetett lejárati idő (Felh.) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Felbontatlan injekciós üvegek
Hűtőszekrényben (2 °C - 8 °C) tárolandó.
Feloldott és hígított oldatok
Az elkészített oldat nem tárolható, hanem azonnal fel kell hígítani. A hígított oldatot 2 °C és 8 °C között legfeljebb 24 órán át lehet tárolni.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz az Fabrazyme?
- A készítmény hatóanyaga: 5 mg béta-agalzidáz injekciós üvegenként. A feloldást követően egy injekciós üveg 5 mg béta-agalzidázt tartalmaz milliliterenként
- Az egyéb összetevők:
-- mannit (E421)
-- nátrium-dihidrogén-foszfát-monohidrát (339)
-- dinátrium-hidrogén-foszfát-heptahidrát (339)
Milyen a Fabrazyme külleme és mit tartalmaz a csomagolás?
A Fabrazyme liofilizált, fehér vagy törtfehér por formájában kerül forgalomba. Feloldást követően tiszta, színtelen folyadék, idegen anyagtól mentes. Az elkészített oldatot tovább kell hígítani.
Kiszerelési egységek: 1 db, 5 db vagy 10 db injekciós üveg dobozonként. Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Fogyasztói ár:
147474Ft
A feltüntetett ár tájékoztató jellegű, patikánként kisebb-nagyobb eltérés előfordulhat.
Normatív támogatás esetén téritési díj: 147474 Ft
 Az adatokat a PHARMINDEX gyógyszer-információs adatbázis szolgáltatja. © Vidal Next Kft. 2026
Az adatokat a PHARMINDEX gyógyszer-információs adatbázis szolgáltatja. © Vidal Next Kft. 2026



















