
LUVERIS 75 NE por és oldószer oldatos injekcióhoz
LUVERIS 75 NE por és oldószer oldatos injekcióhoz betegtájékoztatója
1. Milyen típusú gyógyszer a Luveris és milyen betegségek esetén alkalmazható?
Milyen típusú gyógyszer a Luveris?
A Luveris hatóanyaga az alfa-lutropin, egy rekombináns technológiával készült luteinizáló hormon (LH), mely alapvetően azonos az emberben található hormonnal, de ezt biotechnológiai úton állítják elő. Az úgynevezett gonadotrop hormonok családjába tartozik, melyek a természetes szaporodás szabályozásában játszanak szerepet.
Milyen betegségek esetén alkalmazható a Luveris?
A Luveris-injekciót olyan felnőtt nők kezelésére használják, akikben néhány, a természetes szaporodási ciklusban szerepet játszó hormonból nagyon kevés termelődik. A gyógyszert általában egy másik hormonnal, az úgynevezett tüszőérést serkentő hormonnal, az FSH-val együtt alkalmazzák, mely a petefészekben a tüszőérést és ezzel a petesejtérést segíti elő. Ezt követi egy, egyszeri dózisban adott humán koriogonadotropin hormon (hCG) adása, mely elősegíti a petesejt felszabadulását a tüszőből (az ovulációt).
2. Tudnivalók a Luveris alkalmazása előtt
Ne alkalmazza a Luverist
- ha allergiás a gonadotropinokra (például luteinizáló hormonra, tüszőérést serkentő hormonra vagy humán koriogonadotropinra) vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére,
- ha Önnek petefészek-, méh- vagy emlőrákja van,
- ha Önnél agydaganatot állapítottak meg,
- ha ismeretlen eredetű petefészek-megnagyobbodásban vagy petefészekcisztás megbetegedésben (a petefészekben folyadékkal telt tömlők találhatók) szenved,
- ha ismeretlen eredetű hüvelyi vérzése van.
Ne alkalmazza a Luverist, ha bármely fent említett eset igaz Önre. Amennyiben bizonytalan ebben, a gyógyszer alkalmazása előtt kérdezze meg kezelőorvosát vagy gyógyszerészét.
Figyelmeztetések és óvintézkedések
A Luveris alkalmazása előtt beszéljen kezelőorvosával, gyógyszerészével vagy a gondozását végző egészségügyi szakemberrel.
Az Ön és partnere fogamzó-, illetve termékenyítő képességét a kezelés előtt meg kell határozni.
A Luveris alkalmazása nem javasolt, ha olyan állapot áll fenn, amely a normál terhességet lehetetlenné teszi, például primer petefészek-elégtelenség esetén, aminek következtében a petefészkek nem működnek, vagy a nemi szervek fejlődési rendellenességei esetén.
Porfíria
A kezelés megkezdése előtt tájékoztassa kezelőorvosát, amennyiben Ön vagy családjának bármely tagja porfíriában szenved (a porfirin lebontásának zavara, amelyet a gyermek örökölhet a szülőtől).
Petefészek-hiperstimulációs szindróma (OHSS)
Ez a készítmény serkenti a petefészek működését. Ezért megnöveli a petefészek-hiperstimulációs szindróma, más néven OHSS kialakulásának veszélyét. Ebben az állapotban túl sok tüsző alakul ki és nagy tömlőkké fejlődnek. Amennyiben hasi fájdalma jelentkezik, gyorsan kialakuló testsúlynövekedést, hányingert tapasztal vagy hányás jelentkezik, esetleg nehézlégzése van, azonnal értesítse kezelőorvosát, aki lehetséges, hogy meg fogja kérni Önt a kezelés leállítására (lásd 4. pont, a "Súlyos mellékhatások" alatt).
Amennyiben Önnek nincs ovulációja (nem érik meg petesejtje) és az ajánlott adagot és adagolási módot betartja, az OHSS kialakulása kevésbé valószínű. A Luverisszel történő kezelés ritkán vezethet súlyos OHSS-hez. Ez valószínűbb, ha a tüsző repedését és a petesejt kiszabadulását kiváltó gyógyszerrel (humán koriogonadotropint, hCG-t tartalmazó injekcióval) együtt alkalmazzák (lásd 3. pont, a "Milyen gyakran kell alkalmazni a készítményt?" kérdés alatt). Amennyiben Önnél OHSS alakul ki, ebben a kezelési ciklusban célszerű mellőzni a hCG-t, továbbá kezelőorvosa kérésére a nemi életet szüneteltetni, vagy mechanikus fogamzásgátló eszközökkel védekezni legalább 4 napon keresztül.
Kezelőorvosa ellenőrizni fogja a petefészek működését a kezelés előtt és alatt, ultrahangos vizsgálattal és vérvétellel.
Többszörös terhesség
A Luveris alkalmazása során nagyobb valószínűséggel alakul ki olyan terhesség, ahol egynél több magzat van jelen ("többszörös terhesség", leggyakrabban kettős iker), mint a természetes úton történő teherbeesés során. A többszörös terhesség Önt és a magzatokat is érintő szövődményekkel járhat. A Luveris megfelelő adagjának a megfelelő időben történő alkalmazásával csökkentheti a többszörös terhesség kialakulásának valószínűségét. Amennyiben asszisztált reprodukciós kezeléseken vesz részt, a többszörös terhesség kialakulásának valószínűsége függ az Ön életkorától, a megtermékenyített petesejtek és a visszaültetett embriók számától és életképességétől.
Vetélés
Amennyiben asszisztált reprodukciós kezeléseken vagy petesejtérést elősegítő kezelésen esik át, Önnél nagyobb a vetélés valószínűsége, mint az átlagnépességben.
Méhen kívüli terhesség
Azoknál a nőknél, akik korábban petevezeték-betegségben szenvedtek, fennáll a méhen kívüli terhesség (olyan terhesség, amelyben az embrió a méhen kívül ágyazódik be) kockázata, függetlenül attól, hogy természetes fogamzással vagy a megtermékenyítést elősegítő kezelés során jött létre a terhesség.
Véralvadási zavarok (tromboembóliás események)
Beszéljen kezelőorvosával a Luveris alkalmazása előtt, ha Önnél vagy bármelyik családtagjánál valaha előfordult vérrög a láb vagy a tüdő ereiben, illetve előfordult szívroham vagy agyi érkatasztrófa (stroke, sztrók). Lehetséges, hogy Önnél nagyobb valószínűséggel alakulnak ki súlyos vérrögök vagy súlyosbodhatnak a már létező vérrögök a Luveris-kezelés során.
A nemi szervek daganatos megbetegedései
Beszámoltak rosszindulatú és jóindulatú petefészekdaganatok, valamint egyéb nemi szervi daganatok előfordulásáról olyan nők esetében, akik meddőség miatt többször estek át gyógyszeres kezelésen.
Veleszületett rendellenességek
Veleszületett rendellenességek előfordulása az asszisztált reprodukciós kezelések alkalmazása után kicsit magasabb lehet, mint természetes fogamzás után. Ez lehet a szülői tényezők különbségei miatt, mint például anyai életkor, genetika, valamint az asszisztált reprodukciós kezelés beavatkozása miatt, vagy a többszörös terhesség miatt.
Gyermekek és serdülők
A Luveris nem alkalmazható gyermekek és 18 évnél fiatalabb serdülők kezelésére.
Egyéb gyógyszerek és a Luveris
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről.
Ne alkalmazza a Luverist más gyógyszerekkel összekeverve ugyanabban az injekcióban, kivéve az alfa-follitropinnal, ha kezelőorvosa ezt írta fel Önnek.
Terhesség és szoptatás
Ne alkalmazzon Luverist, ha terhes vagy szoptat.
Mielőtt bármilyen gyógyszert elkezdene szedni, beszélje meg kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
A Luveris nem, vagy csak elhanyagolható mértékben befolyásolja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességeket.
A Luveris nátriumot tartalmaz
A Luveris kevesebb mint 1 mmol (23 mg) nátriumot tartalmaz adagonként, azaz gyakorlatilag "nátriummentes".
3. Hogyan kell alkalmazni a Luverist?
A gyógyszert mindig a kezelőorvosa által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát.
Hogyan kell alkalmazni a készítményt?
A kezelőorvos határozza meg az Önnek optimális adagot és a kezelés menetét, időtartamát.
Az oldószert ampullában tartalmazó kiszerelés esetén:
A betegek részére rendelkezésre áll az otthoni alkalmazást jobban elősegítő, felhasználóbarát kiszerelés. Beszélje meg kezelőorvosával, milyen más, megfelelőbb módszer érhető el az Ön számára.
Milyen gyakran kell alkalmazni a készítményt?
A Luverist az FSH-injekcióval együtt három héten át minden nap be kell adni.
- A szokásos kezdőadag 75 NE (1 injekciós üveg) Luveris-injekció, 75 NE vagy 150 NE FSH-val együtt.
- Az Ön reakciójától függően a kezelőorvos növelheti az FSH-adagot 37,5 - 75 NE-gel 7 - 14 napos időközökben.
A kezelőorvos a kezelést 5 hétre kiterjesztheti.
Amikor már megfelelően reagál a kezelésre, egy adag hCG-t kap az utolsó Luveris- és FSH-injekciót követő 24 - 48 órán belül. Ajánlott a hCG beadásának napján és másnapján házaséletet élni. Alternatív megoldásként, kezelőorvosa megítélése alapján, mesterséges megtermékenyítés vagy más, orvosilag támogatott reprodukciós kezelés is végezhető.
Ha túlzott mértékben reagál a gyógyszerre, a kezelést le kell állítani és a hCG adását fel kell függeszteni (lásd 4. pont, "Petefészek-hiperstimulációs szindróma (OHSS)" alatt). A következő ciklusban a kezelőorvos újrakezdi a kezelést alacsonyabb FSH-adag mellett, mint amilyet az előző ciklus során alkalmazott.
Az alkalmazás módja
A Luveris-injekciót szubkután kell beadni, vagyis a bőr alá. Minden injekciós üvegben csak egy adag injekció van.
Az oldószert ampullában tartalmazó kiszerelés esetén:
Ha Ön magának adja be a Luveris-injekciót, olvassa el figyelmesen az alábbi utasításokat:
- Mossa meg a kezét. Fontos, hogy a keze és a használt eszközök tiszták legyenek.
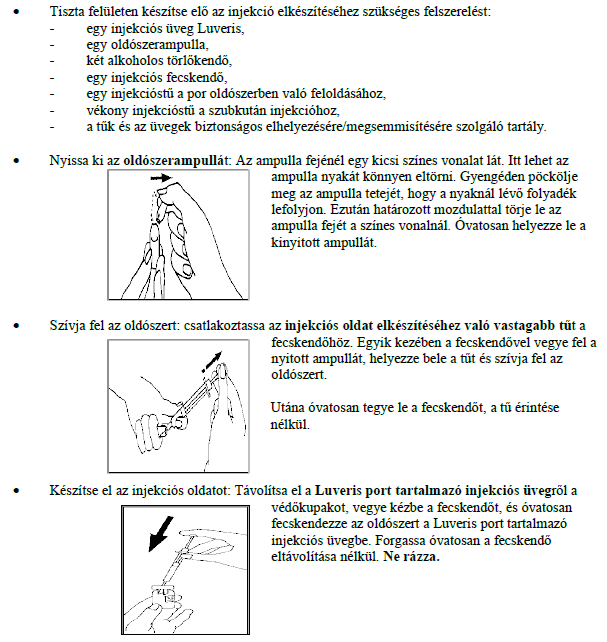
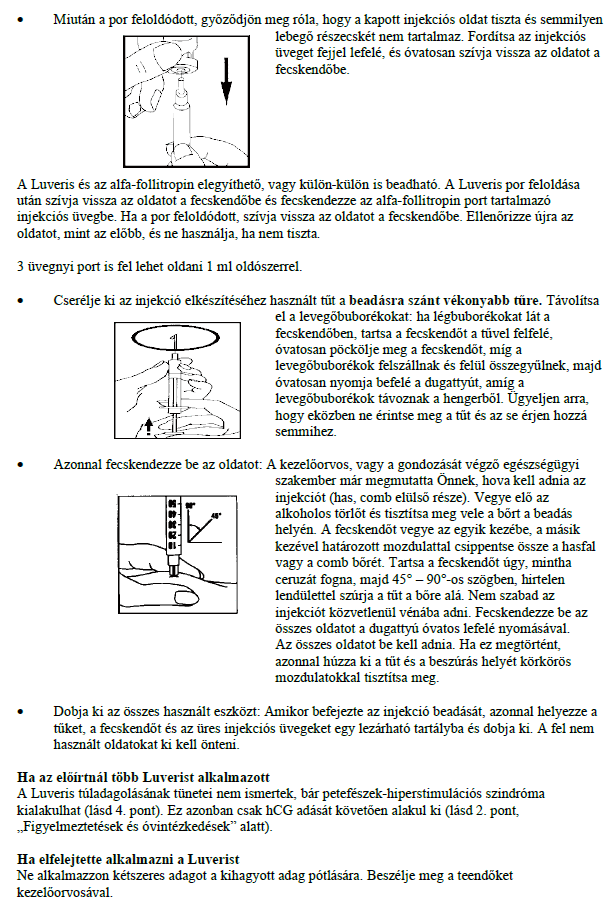
Az oldószert injekciós üvegben tartalmazó kiszerelés esetén:
Ha Ön magának adja be a Luveris-injekciót, olvassa el figyelmesen az alábbi utasításokat:
- Mossa meg a kezét. Fontos, hogy a keze és a használt eszközök tiszták legyenek.
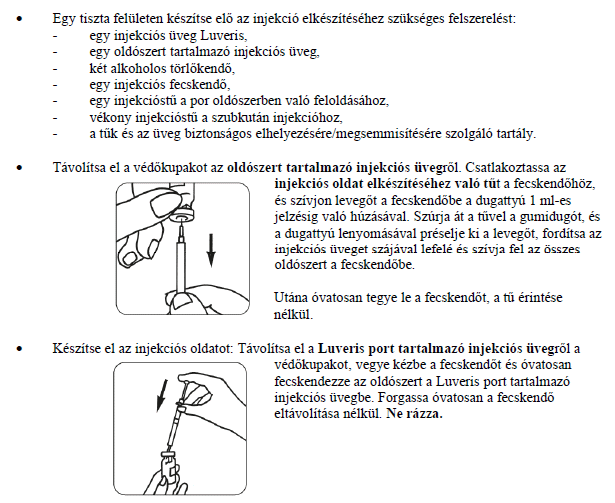

Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Súlyos mellékhatások
Ha az alább felsorolt mellékhatások valamelyike jelentkezik Önnél, azonnal értesítse kezelőorvosát. Lehetséges, hogy kezelőorvosa a Luveris alkalmazásának abbahagyására fogja kérni Önt.
Allergiás reakció
Az olyan allergiás reakciók, mint a bőrkiütés, a bőrvörösség, a csalánkiütés, az arc feldagadása nehézlégzéssel társulva alkalmanként súlyossá válhatnak. Ezek a mellékhatások nagyon ritkán jelentkeznek (10 000 betegből legfeljebb 1 beteget érinthet).
Petefészek-hiperstimulációs szindróma (OHSS)
- Alhasi fájdalom hányingerrel vagy hányással társulva a petefészek-hiperstimulációs szindróma (OHSS) tünete lehet. Lehetséges, hogy a kezelésre túlzott választ adott az Ön petefészke, és nagy folyadékgyülem vagy ciszták alakultak ki (lásd 2. pont, "Petefészek-hiperstimulációs szindróma (OHSS)" alatt). Ez a mellékhatás gyakran kialakul (10 betegből legfeljebb 1 beteget érinthet). Ha Önnél is kialakul, fontos, hogy kezelőorvosa a lehető leghamarabb megvizsgálja Önt.
- Nagyon ritkán, általában súlyos OHSS-sel együtt, súlyos véralvadási szövődmények (tromboembóliás események) alakulnak ki. Ez mellkasi fájdalmat, légszomjat, agyi érkatasztrófát (stroke, sztrók) vagy szívrohamot válthat ki (lásd 2. pont, "Véralvadási zavarok" alatt).
Egyéb gyakori mellékhatások
- Fejfájás;
- hányinger, hányás, hasmenés, kellemetlen hasi érzés vagy hasi fájdalom;
- folyadékgyülem a petefészekben (petefészekciszták), emlőfájdalom és kismedencei fájdalom;
- helyi reakciók az injekció beadásának helyén, mint például fájdalom, viszketés, véraláfutás, duzzanat vagy irritáció.
Petefészek-csavarodást (torziót) és hasüregbe való vérzést nem tapasztaltak a Luveris adását követően, bár egy vizeletből előállított, szintén LH-t tartalmazó gyógyszerrel, a human menopauzális gonadotropinnal (hMG) történő kezelést követően már jelentettek ilyen mellékhatást.
Méhen kívüli terhesség (az embrió a méhen kívül ágyazódik be) is kialakulhat, különösen olyan nőknél, akiknek a kórelőzményében a petevezeték megbetegedése szerepel.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a https://mellekhatas.ogyei.gov.hu/ weboldalon. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Luverist tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A dobozon és az injekciós üvegeken feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Legfeljebb 25 °C-on tárolandó. A fénytől való védelem érdekében az eredeti csomagolásban tárolandó.
Ne alkalmazza ezt a gyógyszert, ha a por elszíneződött, illetve ha megsérült a csomagolás.
Az injekciót az elkészítés után azonnal be kell adni.
Az elkészített injekciót nem szabad beadni, ha lebegő részecskét tartalmaz, vagy ha nem tiszta.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Luveris?
- A készítmény hatóanyaga: alfa-lutropin. Egy injekciós üveg 75 NE-t (nemzetközi egység) tartalmaz.
- Az alfa-lutropin rekombináns humán luteinizáló hormon (r-hLH), amelyet rekombináns DNS-technológiával állítanak elő.
- A por egyéb összetevői: poliszorbát 20, szacharóz, nátrium-dihidrogén-foszfát-monohidrát, dinátrium-hidrogén-foszfát-dihidrát, tömény foszforsav, nátrium-hidroxid, L-metionin, nitrogén.
- Oldószer: injekcióhoz való víz.
Milyen a Luveris külleme és mit tartalmaz a csomagolás?
- A Luveris por és oldószer formájában kerül forgalomba.
Az oldószert ampullában tartalmazó kiszerelés esetén:
- Minden port tartalmazó injekciós üvegben 75 NE alfa-lutropin van, valamint minden oldószerampulla 1 ml injekcióhoz való vizet tartalmaz.
- A Luveris csomagolásának tartalma: 1 db, 3 db vagy 10 db port tartalmazó injekciós üveg és ugyanannyi oldószerampulla.
Az oldószert injekciós üvegben tartalmazó kiszerelés esetén:
- Minden port tartalmazó injekciós üvegben 75 NE alfa-lutropin van, valamint minden oldószert tartalmazó injekciós üveg 1 ml injekcióhoz való vizet tartalmaz.
- A Luveris csomagolásának tartalma: 1 db, 3 db vagy 10 db port tartalmazó injekciós üveg és ugyanannyi oldószert tartalmazó injekciós üveg.
Milyen típusú gyógyszer a Luveris?
A Luveris hatóanyaga az alfa-lutropin, egy rekombináns technológiával készült luteinizáló hormon (LH), mely alapvetően azonos az emberben található hormonnal, de ezt biotechnológiai úton állítják elő. Az úgynevezett gonadotrop hormonok családjába tartozik, melyek a természetes szaporodás szabályozásában játszanak szerepet.
Milyen betegségek esetén alkalmazható a Luveris?
A Luveris-injekciót olyan felnőtt nők kezelésére használják, akikben néhány, a természetes szaporodási ciklusban szerepet játszó hormonból nagyon kevés termelődik. A gyógyszert általában egy másik hormonnal, az úgynevezett tüszőérést serkentő hormonnal, az FSH-val együtt alkalmazzák, mely a petefészekben a tüszőérést és ezzel a petesejtérést segíti elő. Ezt követi egy, egyszeri dózisban adott humán koriogonadotropin hormon (hCG) adása, mely elősegíti a petesejt felszabadulását a tüszőből (az ovulációt).
2. Tudnivalók a Luveris alkalmazása előtt
Ne alkalmazza a Luverist
- ha allergiás a gonadotropinokra (például luteinizáló hormonra, tüszőérést serkentő hormonra vagy humán koriogonadotropinra) vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére,
- ha Önnek petefészek-, méh- vagy emlőrákja van,
- ha Önnél agydaganatot állapítottak meg,
- ha ismeretlen eredetű petefészek-megnagyobbodásban vagy petefészekcisztás megbetegedésben (a petefészekben folyadékkal telt tömlők találhatók) szenved,
- ha ismeretlen eredetű hüvelyi vérzése van.
Ne alkalmazza a Luverist, ha bármely fent említett eset igaz Önre. Amennyiben bizonytalan ebben, a gyógyszer alkalmazása előtt kérdezze meg kezelőorvosát vagy gyógyszerészét.
Figyelmeztetések és óvintézkedések
A Luveris alkalmazása előtt beszéljen kezelőorvosával, gyógyszerészével vagy a gondozását végző egészségügyi szakemberrel.
Az Ön és partnere fogamzó-, illetve termékenyítő képességét a kezelés előtt meg kell határozni.
A Luveris alkalmazása nem javasolt, ha olyan állapot áll fenn, amely a normál terhességet lehetetlenné teszi, például primer petefészek-elégtelenség esetén, aminek következtében a petefészkek nem működnek, vagy a nemi szervek fejlődési rendellenességei esetén.
Porfíria
A kezelés megkezdése előtt tájékoztassa kezelőorvosát, amennyiben Ön vagy családjának bármely tagja porfíriában szenved (a porfirin lebontásának zavara, amelyet a gyermek örökölhet a szülőtől).
Petefészek-hiperstimulációs szindróma (OHSS)
Ez a készítmény serkenti a petefészek működését. Ezért megnöveli a petefészek-hiperstimulációs szindróma, más néven OHSS kialakulásának veszélyét. Ebben az állapotban túl sok tüsző alakul ki és nagy tömlőkké fejlődnek. Amennyiben hasi fájdalma jelentkezik, gyorsan kialakuló testsúlynövekedést, hányingert tapasztal vagy hányás jelentkezik, esetleg nehézlégzése van, azonnal értesítse kezelőorvosát, aki lehetséges, hogy meg fogja kérni Önt a kezelés leállítására (lásd 4. pont, a "Súlyos mellékhatások" alatt).
Amennyiben Önnek nincs ovulációja (nem érik meg petesejtje) és az ajánlott adagot és adagolási módot betartja, az OHSS kialakulása kevésbé valószínű. A Luverisszel történő kezelés ritkán vezethet súlyos OHSS-hez. Ez valószínűbb, ha a tüsző repedését és a petesejt kiszabadulását kiváltó gyógyszerrel (humán koriogonadotropint, hCG-t tartalmazó injekcióval) együtt alkalmazzák (lásd 3. pont, a "Milyen gyakran kell alkalmazni a készítményt?" kérdés alatt). Amennyiben Önnél OHSS alakul ki, ebben a kezelési ciklusban célszerű mellőzni a hCG-t, továbbá kezelőorvosa kérésére a nemi életet szüneteltetni, vagy mechanikus fogamzásgátló eszközökkel védekezni legalább 4 napon keresztül.
Kezelőorvosa ellenőrizni fogja a petefészek működését a kezelés előtt és alatt, ultrahangos vizsgálattal és vérvétellel.
Többszörös terhesség
A Luveris alkalmazása során nagyobb valószínűséggel alakul ki olyan terhesség, ahol egynél több magzat van jelen ("többszörös terhesség", leggyakrabban kettős iker), mint a természetes úton történő teherbeesés során. A többszörös terhesség Önt és a magzatokat is érintő szövődményekkel járhat. A Luveris megfelelő adagjának a megfelelő időben történő alkalmazásával csökkentheti a többszörös terhesség kialakulásának valószínűségét. Amennyiben asszisztált reprodukciós kezeléseken vesz részt, a többszörös terhesség kialakulásának valószínűsége függ az Ön életkorától, a megtermékenyített petesejtek és a visszaültetett embriók számától és életképességétől.
Vetélés
Amennyiben asszisztált reprodukciós kezeléseken vagy petesejtérést elősegítő kezelésen esik át, Önnél nagyobb a vetélés valószínűsége, mint az átlagnépességben.
Méhen kívüli terhesség
Azoknál a nőknél, akik korábban petevezeték-betegségben szenvedtek, fennáll a méhen kívüli terhesség (olyan terhesség, amelyben az embrió a méhen kívül ágyazódik be) kockázata, függetlenül attól, hogy természetes fogamzással vagy a megtermékenyítést elősegítő kezelés során jött létre a terhesség.
Véralvadási zavarok (tromboembóliás események)
Beszéljen kezelőorvosával a Luveris alkalmazása előtt, ha Önnél vagy bármelyik családtagjánál valaha előfordult vérrög a láb vagy a tüdő ereiben, illetve előfordult szívroham vagy agyi érkatasztrófa (stroke, sztrók). Lehetséges, hogy Önnél nagyobb valószínűséggel alakulnak ki súlyos vérrögök vagy súlyosbodhatnak a már létező vérrögök a Luveris-kezelés során.
A nemi szervek daganatos megbetegedései
Beszámoltak rosszindulatú és jóindulatú petefészekdaganatok, valamint egyéb nemi szervi daganatok előfordulásáról olyan nők esetében, akik meddőség miatt többször estek át gyógyszeres kezelésen.
Veleszületett rendellenességek
Veleszületett rendellenességek előfordulása az asszisztált reprodukciós kezelések alkalmazása után kicsit magasabb lehet, mint természetes fogamzás után. Ez lehet a szülői tényezők különbségei miatt, mint például anyai életkor, genetika, valamint az asszisztált reprodukciós kezelés beavatkozása miatt, vagy a többszörös terhesség miatt.
Gyermekek és serdülők
A Luveris nem alkalmazható gyermekek és 18 évnél fiatalabb serdülők kezelésére.
Egyéb gyógyszerek és a Luveris
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről.
Ne alkalmazza a Luverist más gyógyszerekkel összekeverve ugyanabban az injekcióban, kivéve az alfa-follitropinnal, ha kezelőorvosa ezt írta fel Önnek.
Terhesség és szoptatás
Ne alkalmazzon Luverist, ha terhes vagy szoptat.
Mielőtt bármilyen gyógyszert elkezdene szedni, beszélje meg kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
A Luveris nem, vagy csak elhanyagolható mértékben befolyásolja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességeket.
A Luveris nátriumot tartalmaz
A Luveris kevesebb mint 1 mmol (23 mg) nátriumot tartalmaz adagonként, azaz gyakorlatilag "nátriummentes".
3. Hogyan kell alkalmazni a Luverist?
A gyógyszert mindig a kezelőorvosa által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát.
Hogyan kell alkalmazni a készítményt?
A kezelőorvos határozza meg az Önnek optimális adagot és a kezelés menetét, időtartamát.
Az oldószert ampullában tartalmazó kiszerelés esetén:
A betegek részére rendelkezésre áll az otthoni alkalmazást jobban elősegítő, felhasználóbarát kiszerelés. Beszélje meg kezelőorvosával, milyen más, megfelelőbb módszer érhető el az Ön számára.
Milyen gyakran kell alkalmazni a készítményt?
A Luverist az FSH-injekcióval együtt három héten át minden nap be kell adni.
- A szokásos kezdőadag 75 NE (1 injekciós üveg) Luveris-injekció, 75 NE vagy 150 NE FSH-val együtt.
- Az Ön reakciójától függően a kezelőorvos növelheti az FSH-adagot 37,5 - 75 NE-gel 7 - 14 napos időközökben.
A kezelőorvos a kezelést 5 hétre kiterjesztheti.
Amikor már megfelelően reagál a kezelésre, egy adag hCG-t kap az utolsó Luveris- és FSH-injekciót követő 24 - 48 órán belül. Ajánlott a hCG beadásának napján és másnapján házaséletet élni. Alternatív megoldásként, kezelőorvosa megítélése alapján, mesterséges megtermékenyítés vagy más, orvosilag támogatott reprodukciós kezelés is végezhető.
Ha túlzott mértékben reagál a gyógyszerre, a kezelést le kell állítani és a hCG adását fel kell függeszteni (lásd 4. pont, "Petefészek-hiperstimulációs szindróma (OHSS)" alatt). A következő ciklusban a kezelőorvos újrakezdi a kezelést alacsonyabb FSH-adag mellett, mint amilyet az előző ciklus során alkalmazott.
Az alkalmazás módja
A Luveris-injekciót szubkután kell beadni, vagyis a bőr alá. Minden injekciós üvegben csak egy adag injekció van.
Az oldószert ampullában tartalmazó kiszerelés esetén:
Ha Ön magának adja be a Luveris-injekciót, olvassa el figyelmesen az alábbi utasításokat:
- Mossa meg a kezét. Fontos, hogy a keze és a használt eszközök tiszták legyenek.


Az oldószert injekciós üvegben tartalmazó kiszerelés esetén:
Ha Ön magának adja be a Luveris-injekciót, olvassa el figyelmesen az alábbi utasításokat:
- Mossa meg a kezét. Fontos, hogy a keze és a használt eszközök tiszták legyenek.


Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Súlyos mellékhatások
Ha az alább felsorolt mellékhatások valamelyike jelentkezik Önnél, azonnal értesítse kezelőorvosát. Lehetséges, hogy kezelőorvosa a Luveris alkalmazásának abbahagyására fogja kérni Önt.
Allergiás reakció
Az olyan allergiás reakciók, mint a bőrkiütés, a bőrvörösség, a csalánkiütés, az arc feldagadása nehézlégzéssel társulva alkalmanként súlyossá válhatnak. Ezek a mellékhatások nagyon ritkán jelentkeznek (10 000 betegből legfeljebb 1 beteget érinthet).
Petefészek-hiperstimulációs szindróma (OHSS)
- Alhasi fájdalom hányingerrel vagy hányással társulva a petefészek-hiperstimulációs szindróma (OHSS) tünete lehet. Lehetséges, hogy a kezelésre túlzott választ adott az Ön petefészke, és nagy folyadékgyülem vagy ciszták alakultak ki (lásd 2. pont, "Petefészek-hiperstimulációs szindróma (OHSS)" alatt). Ez a mellékhatás gyakran kialakul (10 betegből legfeljebb 1 beteget érinthet). Ha Önnél is kialakul, fontos, hogy kezelőorvosa a lehető leghamarabb megvizsgálja Önt.
- Nagyon ritkán, általában súlyos OHSS-sel együtt, súlyos véralvadási szövődmények (tromboembóliás események) alakulnak ki. Ez mellkasi fájdalmat, légszomjat, agyi érkatasztrófát (stroke, sztrók) vagy szívrohamot válthat ki (lásd 2. pont, "Véralvadási zavarok" alatt).
Egyéb gyakori mellékhatások
- Fejfájás;
- hányinger, hányás, hasmenés, kellemetlen hasi érzés vagy hasi fájdalom;
- folyadékgyülem a petefészekben (petefészekciszták), emlőfájdalom és kismedencei fájdalom;
- helyi reakciók az injekció beadásának helyén, mint például fájdalom, viszketés, véraláfutás, duzzanat vagy irritáció.
Petefészek-csavarodást (torziót) és hasüregbe való vérzést nem tapasztaltak a Luveris adását követően, bár egy vizeletből előállított, szintén LH-t tartalmazó gyógyszerrel, a human menopauzális gonadotropinnal (hMG) történő kezelést követően már jelentettek ilyen mellékhatást.
Méhen kívüli terhesség (az embrió a méhen kívül ágyazódik be) is kialakulhat, különösen olyan nőknél, akiknek a kórelőzményében a petevezeték megbetegedése szerepel.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a https://mellekhatas.ogyei.gov.hu/ weboldalon. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Luverist tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A dobozon és az injekciós üvegeken feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Legfeljebb 25 °C-on tárolandó. A fénytől való védelem érdekében az eredeti csomagolásban tárolandó.
Ne alkalmazza ezt a gyógyszert, ha a por elszíneződött, illetve ha megsérült a csomagolás.
Az injekciót az elkészítés után azonnal be kell adni.
Az elkészített injekciót nem szabad beadni, ha lebegő részecskét tartalmaz, vagy ha nem tiszta.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Luveris?
- A készítmény hatóanyaga: alfa-lutropin. Egy injekciós üveg 75 NE-t (nemzetközi egység) tartalmaz.
- Az alfa-lutropin rekombináns humán luteinizáló hormon (r-hLH), amelyet rekombináns DNS-technológiával állítanak elő.
- A por egyéb összetevői: poliszorbát 20, szacharóz, nátrium-dihidrogén-foszfát-monohidrát, dinátrium-hidrogén-foszfát-dihidrát, tömény foszforsav, nátrium-hidroxid, L-metionin, nitrogén.
- Oldószer: injekcióhoz való víz.
Milyen a Luveris külleme és mit tartalmaz a csomagolás?
- A Luveris por és oldószer formájában kerül forgalomba.
Az oldószert ampullában tartalmazó kiszerelés esetén:
- Minden port tartalmazó injekciós üvegben 75 NE alfa-lutropin van, valamint minden oldószerampulla 1 ml injekcióhoz való vizet tartalmaz.
- A Luveris csomagolásának tartalma: 1 db, 3 db vagy 10 db port tartalmazó injekciós üveg és ugyanannyi oldószerampulla.
Az oldószert injekciós üvegben tartalmazó kiszerelés esetén:
- Minden port tartalmazó injekciós üvegben 75 NE alfa-lutropin van, valamint minden oldószert tartalmazó injekciós üveg 1 ml injekcióhoz való vizet tartalmaz.
- A Luveris csomagolásának tartalma: 1 db, 3 db vagy 10 db port tartalmazó injekciós üveg és ugyanannyi oldószert tartalmazó injekciós üveg.
Fogyasztói ár:
8529Ft
A feltüntetett ár tájékoztató jellegű, patikánként kisebb-nagyobb eltérés előfordulhat.
Kiemelt támogatás esetén térítési díj: 300 Ft
Normatív támogatás esetén téritési díj: 3838 Ft
 Az adatokat a PHARMINDEX gyógyszer-információs adatbázis szolgáltatja. © Vidal Next Kft. 2024
Az adatokat a PHARMINDEX gyógyszer-információs adatbázis szolgáltatja. © Vidal Next Kft. 2024























